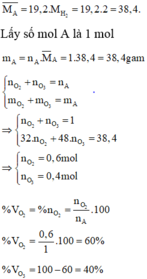Hỗn hợp X gồm O2 và O3 có tỉ khối so với H2 bằng 18.
a. Tính % theo thể tích hỗn hợp
b. Tính % khối lượng hỗn hợp
c. Tính thể tích oxi có trong 22,4 lít hỗn hợp khí trên?
d. Tính khối lượng của 4,48 lít khí X trên?
Mọi người giúp mình với ạ. Mình cảm ơn nhiều.